Travaux Dirigés Physique 1ère D fiche 1 (Notion de quantité de chaleur)
TRAVAUX DIRIGES PHYSIQUE PREMIERE D ET F
THEME : NOTION DE QUANTITE DE CHALEUR
On donne :
Chaleur massique de l’eau : Ce = 4185 J/Kg.K
Chaleur massique de l’aluminium : Ce = 890 J/Kg.K
Chaleur massique de la glace : Cg =2090 J/Kg.K
Chaleur latente de fusion de la glace (0°C) : Lf = 3,3.105 J/Kg
Chaleur latente de vaporisation de l’eau : Lv = 2260 KJ/Kg
Masse volumique de l’eau : ρ = 1000 Kg/m3
chaleur massique du cuivre c = 380 J.kg-1.K-1
Partie I : Evaluation des ressources
Exercice 0: Evaluation des savoirs
1. Définir : Quantité de chaleur ; enceinte adiabatique, capacité thermique massique.
2. Enoncer le principe des échanges de chaleur.
3. Comment appelle t- on le phénomène pour une eau chauffée pendant longtemps à température élevée de se mettre en mouvement ?
4. Citer les différents modes de transfert de chaleur.
5. Répond par « vrai » ou « faux »
5.1 L’énergie, le travail et la quantité de chaleur s’expriment avec la même unité.
5.2 Une quantité de chaleur est toujours positive.
5.3 Pendant l’ébullition de l’eau pure, la température reste constante : l’eau n’absorbe pas la chaleur pendant l’ébullition.
Exercice 1
Une casserole en aluminium de masse M = 200 g renferme 1,5 litre d’eau à la température initiale T1 = 70°C. On laisse refroidir l’ensemble jusqu’à la température T2 = 30°C.
1. Déterminer la masse m1 de l’eau
2. Déterminer la capacité thermique C du système (casserole-eau)
Exercice 2
On prélève un morceau de glace de masse m = 50 g dans un congélateur où la température vaut T1 = -10°C. On l’abandonne sur un plat dans une pièce où la température est maintenue constante et égale à T2 = 2O°C.
1. Déterminer les phases successives lors de l’évolution du morceau de glace. Quel est son état initial ?
2. Calculer l’énergie transférée au morceau de glace.
Exercice 3
On veut obtenir 10 litres d’eau distillée en chauffant de l’eau du robinet prise à 15°C.
1. Déterminer la variation d’énergie calorifique de 1O litres d’eau liquide qui passe de 15°C à 100°C.
2. Déterminer la quantité de chaleur qui pourra transformer cette eau en vapeur à 100°C sous la pression de 1 bar.
3. Déterminer la quantité de chaleur qu’il a fallu transférer à l’eau pour la faire passer de 15°C à 100°C.
4. On condense la vapeur à l’aide d’un réfrigérateur pour obtenir 10 litres d’eau distillée à 15°C. Déterminer la quantité de chaleur cédée au réfrigérant au cours de cette condensation.
Exercice 4
Un chauffe-eau à gaz débite 5 litres d’eau chaude par minute. L’eau entre dans l’appareil à 15°C et en sort à 60°C.
1. Déterminer la quantité de chaleur reçue par l’eau en une heure.
2. Déterminer la consommation horaire de gaz sachant que la combustion de 1 m 3 de gaz fournit 1338 KJ et que les pertes de chaleur représentent 20% de la chaleur provenant de la combustion du gaz.
Exercice 5 :
1. Enoncer le principe des échanges de chaleur.
2. Un calorimètre de capacité calorifique K=180 j.K-1 contient une masse m1=300g d’eau. La température initiale d’équilibre de cet eau est t1=19.8oC. On y plonge un bloc de plomb, de masse m2=265g sortant d’une étuve a la température t2=95oC. La température finale est alors tf=21.5oC. Calculer la capacité thermique massique du plomb. On donne : Ceau=4180 J.Kg-1.oC.
3. Calculer la quantité de chaleur nécessaire pour porter un bloc d’étain de masse m=300g pris a la température T1=18oC a la température T2=320oC sachant que la température de fusion de l’étain est de 232oC. On donne Chaleur massique de l’étain C=2.2x102j/Kg.K chaleur massique de l’étain liquide C’=2.4x102 j/Kg.K ; chaleur latente de fusion de l’étain Lf=6.104 j/Kg.
Exercice 6
1. énoncer le principe des échanges de chaleur.
2. Un calorimètre de capacité calorifique K=180 j.K-1 contient une masse m1=300g d’eau. La température initiale d’équilibre de cet eau est t1=19.8oC. On y plonge un bloc de plomb, de masse m2=265g sortant d’une étuve a la température t2=95oC. la température finale est alors tf=21.5oC. calculer la capacité thermique massique du plomb. On donne : Ceau=4180 J.Kg-1.oC.
3. Calculer la quantité de chaleur nécessaire pour porter un bloc d’étain de masse m=300g pris a la température T1=18oC a la température T2=320oC sachant que la température de fusion de l’étain est de 232oC. On donne Chaleur massique de l’étain C=2.2x102j/Kg.K chaleur massique de l’étain liquide C’=2.4x102 j/Kg.K ; chaleur latente de fusion de l’étain Lf=6.104 j/Kg.
Exercice 7
Un thermomètre, forme d’une tige de verre de masse 20g, et contenant 0.6cm3 de mercure, est plongé dans un calorimètre en laiton, de masse 100g. Un agitateur en verre, placé dans le calorimètre, a une masse de 15g.
1. calculer la capacité thermique du calorimètre.
2. On appelle valeur en eau du calorimètre, la masse d’eau qui a la même capacité thermique. Calculer cette masse.
3. Pour effectuer une mesure, on introduit 400g d’eau. Peut-on négliger la capacité thermique du calorimètre devant celle de l’eau introduite ?
Donnés : Claiton=370j/kg.K ; Cverre=0,84j/kg.k ; Cmercure=0,14j/g.k ; ρmercure = 13,6g/cm3 ; Ceaau = 4180j/kg.k
EXERCICE : 8
Un calorimètre de capacité calorifique K = 180 J.K-1 contient une masse m1 = 300 g d’eau .la température initiale d’équilibre est ϴ1= 19,8 °C .on y plonge un bloc de plomb, de masse m2 = 265 g sortant d’une étuve à la température ϴ2 = 95 °C, la température finale est ϴf = 21,5 °C, calculer la capacité thermique massique du plomb.
On donne : Ceau = 4180 J.Kg-1. °C-1
EXERCICE : 9
Un calorimètre en cuivre dont la masse est m = 100 g contient m1 = 200 g d’eau à la température ϴ1=4°C on introduit m2 = 300 g de cuivre à la température ϴ2= -20°C on agite le mélange jusqu’à ce que la température soit uniforme.
1- quelle est la température d’équilibre ϴe ?
2- montrer que si le cuivre introduit dans le calorimètre est à la température ϴ ‘2=-50 °C une partie de l’eau se congèle.
3- Calculer alors dans ce cas la masse d’eau congelée
Donnée : chaleur massique du cuivre : C2 = 380 J/Kg/K, de l’eau : Ceau = 4185 J/Kg/K et chaleur de fusion de la glace Lf = 330 KJ /kg
EXERCICE : 10
Une plaque chauffante de cuisinière électrique sert a échauffer 1 L d’eau pris à la température ϴ1= 20°C.
1- Calculer l’énergie Q1 reçue par l’eau si la température finale est ϴf = 80 °C.
2- l’eau reçoit au cours du chauffage 60 % de l’énergie fournie par la plaque
2-1- quelle est la valeur de l’énergie Q fournie par la plaque 2-2-sachant que le verre de la cocote reçoit 25 % de Q , quelle quantité de chaleur reçoit la cocote ?
2-3- que représentent les 15 % d’énergie non reçue par la cocote et l’eau ?
3- calculer la capacité calorifique de l’ensemble [eau + cocotte]
Donnée : capacité thermique de la cocotte : K2 = 20 J/°C
Exercice 11 : Evaluation de savoir-faire et savoir-être
A/ Un calorimètre contient 100g d’eau à 20°C. on ajoute 80g d’eau à 50°C.
1- Quelle serait la température d’équilibre θe si on pouvait négliger la capacité thermique K du calorimètre ?
2- On constata que la température d’équilibre est en réalité θe = 32°C Déterminer K. On donne Ceau= 4,2 kJ.kg-1.K-1.
3- Le même calorimètre contient à présent 100g d’eau à 20°C. On y plonge un échantillon en aluminium, de masse m = 50g, sortant d’une étuve à 90°C. La température d’équilibre étant θe = 26°C, calculer la chaleur massique Cal de l’aluminium.
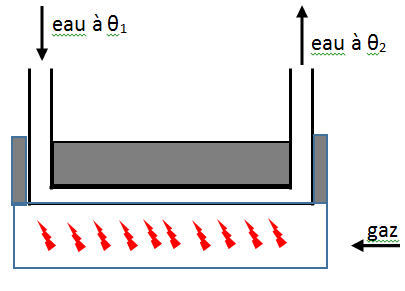
1. Pour alimenter un lave-main, on utilise un chauffe-eau à gaz qui fournit de l’eau chaude avec un débit d = 6 L/min. L’eau pénètre dans un chauffe-eau à θ1 = 25°C avec le même débit. A la sortie, la température de l’eau s’élève à jusqu’à θ2 = 70°C.
1.1Déterminer la quantité de chaleur Q reçue par l’eau pendant t = 2 min.
1.2 L’eau ne reçoit que 75% de l’énergie dégagée par la combustion du gaz.
Déterminer la quantité totale d’énergie W que doit dégager la combustion du gaz en t = 5min.
2. On désire obtenir un bain d’eau tiède à la température θ = 40°C, d’un volume total V = 250 L, en mélangeant un volume V1 d’eau à la température θ1 =80°C et un volume V2 d’eau froide à la température θ2 = 15°C.
Déterminer V1 et V2 en supposant négligeables les fuites thermiques lors du mélange.
3. On prélève un morceau de glace de masse m = 150g dans un congélateur à la température θ1 = -15°C. On transfère à ce glaçon une quantité de chaleur Q = 20kJ.
3.1- Quelle quantité de chaleur doit-on transférer au glaçon pour qu’il atteigne sa température de fusion ?
3.2- Quelle quantité de chaleur doit-on fournir au morceau pris à sa température de fusion pour la rendre totalement liquide ?
3.3- Déterminer l’état final et la température finale du système.
C/ Un récipient en aluminium à usage domestique a une masse m =500g. 1- Quelle est sa capacité thermique ?
2- Le récipient étant initialement à la température θ1 = 20°C. on y introduit un demi-litre d’eau à la température θ2 = 30°C. Quelle est la température finale θ ? On néglige les fuites thermiques.
3- Quelle quantité minimale de chaleur faut-il fournir au système (récipient + eau) pour porter sa température à la valeur θ3 = 80°C ?
4- Pour évaluer les fuites thermiques existant à cette température. On laisse le système se refroidir à l’air libre. Après une minute d’attente, la température est θ4 = 78,5°C. Quelle est la quantité de chaleur perdue par seconde par le système ?
On donne la chaleur massique de l’aluminium c1 = 890 J.kg-1.K-1, la chaleur massique de l’eau c2 = 4,2 kJ.kg-1.K-1.
D/ Dans un calorimètre contenant 100g d’alcool éthylique à la température θ1 = 15°C, on introduit 100g d’alcool à la température θ2 = 25°C. La température finale est θf = 19°C
1- Calculer la capacité thermique et la valeur en eau du calorimètre. Les chaleurs massiques respectives de l’alcool et de l’eau sont 2,4kJ.kg-1.K-1 et 4,2 kJ.kg-1.K-1.
2- On ajoute 100g d’alcool éthylique à 40°C. Quelle est la température finale ?
Partie II : Evaluation des compétences
Situation problème 1 : Abbo fait sortir d’un congélateur, un morceau de viande de masse m1 = 400g à la température θ1= -25°C et le plonge dans un calorimètre de capacité thermique négligeable, contenant une masse m2 = 200g d’eau à la température initiale θ2 = 10°C. Il souhaite déterminer l’état final d’équilibre.
Tâche : Aidez-le à déterminer l’état final d’équilibre du système
Consigne : On calculera la température finale du système, masse des différents corps présents dans le calorimètre). On donne :
• Chaleur massique de l’eau : Ce = 4185 J.kg-1.K-1
• Chaleur massique de la glace : Cg = 2090 J.kg-1.K-1
• Chaleur massique de la viande : Cvi = 460 J.kg-1.K-1
• Chaleur latente de fusion de la glace à 0°C : Lf = 3.34x105 J.kg-1.
Situation problème 2 : M. Appo est un forgeron du village qui fabrique les outils de l’artisanat. Il place dans un four, un morceau de fer de masse 22,3g pour fabriquer une machette. Son enfant Aminou élève en classe de première scientifique après avoir lu son cours sur la notion de quantité de chaleur, souhaite déterminer la température du four. Il fait sortir le morceau de fer du four et le plonge rapidement dans un calorimètre contenant 450g d’eau à 15°C ; il constate que la température de l’eau s’élève jusqu’à 22,5°C. Tâche 1 : Aidez-le à déterminer la température de four si la chaleur massique du fer est de 480 J.kg-1.°C-1.
On donne la chaleur massique de l’eau : Ce = 419 J.kg-1.°C-1
Tâche 2 : Dans la détermination de cette température, on constate qu’on a pas tenu compte de la capacité thermique du calorimètre qui vaut, en réalité 84J.°C-1. Y a-t-il lieu de corriger les résultats ?
Tâche 3 : Quelle est la chaleur massique du liquide si elle décide de remplacer l’eau du calorimètre par un liquide de 100g à la température de 15°C. Le même morceau de fer, préalablement porté à 100°C est plongé dans le liquide dont la température s’élève à 19,1°C.








Commentaires (0)
Laisser un commentaire